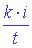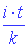| Как изменится сопротивление полупроводников и проводников при введении в них примесных атомов. |
|
| Какие частицы являются носителями тока в электролитах? |
| В каких средах наблюдается перенос вещества при протекании через них электрического тока? |
| В каких средах наблюдается перенос вещества при протекании через них электрического тока? |
| Сколько меди выделится на катоде при электролизе раствора CuSO4, если через раствор протекает 100 Кл электричества? Электрохимический эквивалент меди 0,329 мг/Кл. |
| При силе тока 2,5 А за 20 мин в электрической ванне выделилось 2032,8 мг неопределённого металла. Определить атомную массу металла. |
|
| Какие из приведённых утверждений неверны? |
|
| Экспериментально установлено, что для большинства чистых металлов с ростом температуры сопротивление току увеличивается приблизительно по линейному закону. Это объясняется … |
|
| Какие из перечисленных ниже элементов нужно ввести в качестве примеси в германий, чтобы получить электронную проводимость: фосфор (5), галлий (3), мышьяк (5), индий (3), сурьма (5)? В скобках указана валентность. |
| В каком из ответов правильно указан перечень сред, в которых электрическое сопротивление с ростом температуры возрастает? |
| Определить массу серебра, выделившегося на электроде из раствора АgNO3 в течение 900 с при силе тока 1 А. Электрохимический эквивалент серебра равен 1,118· 10-6. |
| К какому виду самостоятельного разряда относится молния? |
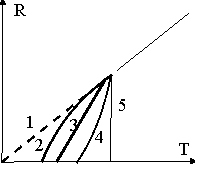 На рисунке показаны 5 графиков зависимости сопротивления проводника R от температуры. Какой из этих графиков выражает явление сверхпроводимости? На рисунке показаны 5 графиков зависимости сопротивления проводника R от температуры. Какой из этих графиков выражает явление сверхпроводимости? |
| Какое количество никеля выделяет ток i = 10 A в течение t = 0,5 час при прохождении через раствор никелевой соли? Электрохимический эквивалент никеля k = 0,3· 10-6 кг/К |
|
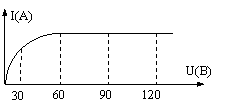 На рисунке изображена вольт - амперная характеристика газа. При каком наименьшем напряжении установился ток насыщения? На рисунке изображена вольт - амперная характеристика газа. При каком наименьшем напряжении установился ток насыщения? |
| Электрический ток в вакууме представляет собой упорядоченное движение |
| Электрический ток в электролитах представляет собой упорядоченное движение |
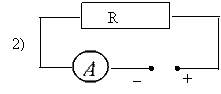
На графике изображена зависимость силы тока от напряжения. К какой из трёх электрических цепей, приведённых ниже, относится эта зависимость?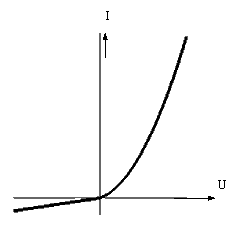 |
|
| Как появляются положительные и отрицательные ионы в водном растворе электролитов? |
| Явление сверхпроводимости металлов было открыто |
|
На рисунке изображена вольтамперная характеристика газа. В каких пределах изменялось напряжение при существовании тока насыщения?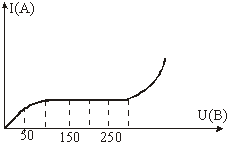 |
| В каких веществах наблюдается явление сверхпроводимости? |
На рисунках приведены вольт - амперные характеристики сред. Какой среде соответствует каждый график ?
| Какие заряженные частицы являются носителями тока в газах ? |
|
| Сколько меди выделится на катоде при электролизе раствора CuSO4, если через раствор протечёт 100 Кл электричества ? Электрохимический эквивалент меди 0,329 мг/Кл. |
| Серебрение пластинок производится при плотности тока j = 0,5 А/дм2, причём за время t = 5 ч выделится масса m = 2 кг серебра. Найти площадь ( м2 ) пластинки. Электрохимический эквивалент серебра К = 1,118·10-6 кг/Кл. |
| Никелирование пластинки проводится при плотности тока 0,4 А/дм2. За какой промежуток времени будет нанесён слой никеля толщины 0,05 мм? Электрохимический эквивалент никеля равен 0,3·10-6 кг/Кл; плотность никеля равна 8,8·103 кг/м3. |
|
| Что возникает при соединении электрона и дырки внутри полупроводника ? |
| Какие действия тока проявляются при любых условиях ? |
|
Четыре электролетические ванны с медными электродами и водным раствором CuSO4 включены в цепь, как показано на рисунке. В каких ваннах будет происходить отложение меди и на каком электроде?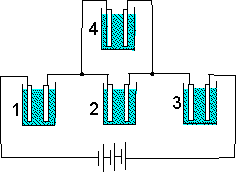 |
Четыре электролетические ванны с медными электродами и водным раствором CuSO4 включены в цепь, как показано на рисунке. Что можно сказать о массах m1,m2, m3, m4 выделевшейся меди в ваннах? |
| При электролизе ZnSO4 выделилось 61,2 г цинка. Определить затраченную энергию электрического тока, если напряжение на зажимах ванны 10 В. Ответ выразить в киловат - часах. |
|
| Определите электрохимический эквивалент хлора, атомная масса которого А = 35,453, валентность n = 1. |
| Определить массу выделившегося хлора при прохождении N = 5·1024 электронов через раствор NaCl. e = 1,6·10-19Кл – заряд электрона, М = 35,45·10-3 кг/моль – молярная масса хлора, n = 1 – валентность хлора, F = 96 500 Кл/моль – число Фарадея. |
| Медный анод массой 33 г погружен в ванну с водным раствором медного купороса. Через сколько времени анод полностью растворится, если электролиз идет при силе тока 2 А? М = 63,55·10-3 кг/моль – молярная масса меди, n = 2 – валентность хлора, F = 96 500 Кл/моль – число Фарадея. |
Как будут светиться лампы Л1 и Л2 при подаче на указанный участок цепи переменного напряжения?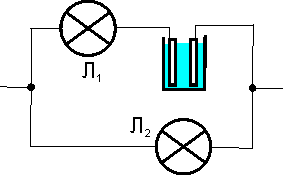 |
Как будут светиться лампы Л1 и Л2 при подаче на указанный участок цепи постоянного напряжения? |
| Покрытие стальных деталей производится двухвалентным никелем при плотности тока в электролитической ванне j = 400 А/м2. Сколько времени потребуется для покрытия детали слоем никеля толщиной 60 мкм? М = 58,71·10-3 кг/моль – молярная масса никеля, n = 2 – валентность никеля, F = 96 500 Кл/моль – число Фарадея, ρ = 8,8·103 кг/м3– плотность никеля, . |
| Две электролитические ванны с растворами CuSO4 и AgNO3 соединены последовательно. Сколько серебра выделится за время, в течение которого выделилось 6,6 г меди? kCu = 3,3·10-7 кг/Кл – электрохимический эквивалент меди, kAg = 1,118·10-8 кг/Кл – электрохимический эквивалент серебра. |
| Почему в водных растворах солей, кислот и щелочей происходит распад молекул растворимых веществ на ионы? |
|
| Сколько серебра выделится на катоде при прохождении через водный раствор азотно-серебряиой соли за 5 ч, если сопротивление ванны 6 Ом, напряжение на ее зажимах 6 В? Серебро одновалентное. М = 107,87·10-3 кг/моль – молярная масса серебра, n = 1 – валентность серебра, F = 96 500 Кл/моль – число Фарадея. |
| Две электролитические ванны соединены последовательно. В первой ванне выделилось 19,5 г цинка, во второй за это же время-11,2 г железа. Цинк двухвалентен. Какова валентность железа? МZn = 65,37·10-3 кг/моль – молярная масса цинка, МFe = 11,20·10-3 кг/моль – молярная масса железа. |
| Как называется физическая величина, равная электрическому заряду, который надо пропустить через раствор электролита, чтобы на электроде выделилась масса вещества, численно равная отношению молярной массы вещества к валентности. |
| При электролизе водного раствора CuS04 была совершена работа 200 кВт·ч. Определить массу полученной меди, если напряжение на зажимах ванны 6 В. М = 63,54·10-3 кг/моль – молярная масса меди, n = 2 – валентность меди, F = 96 500 Кл/моль – число Фарадея. |
| Ванна с раствором азотнокислого серебра подключена к источнику с напряжением 4 В. Определить сопротивление раствора в ванне, если за 1 ч на катоде выделилось 6,04 г серебра. k = 1,118·10-6 кг/Кл – электрохимический эквивалент серебра. |
| Как называется проводник с ионной проводимостью? |
|
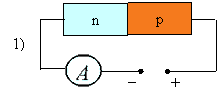
Как будут меняться показания амперметра, если электролит нагреть до определённой температуры?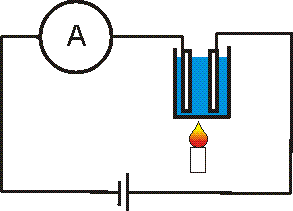 |
| Через раствор серной кислоты прошло 2·105 Кл количества электричества. Определить массу и объем выделившегося водорода при нормальных условиях. Плотность водорода ρо = 9·10-2 кг/м3. М = 1·10-3 кг/моль – молярная масса водорода, n = 1 – валентность водорода, F = 96 500 Кл/моль – число Фарадея. |
| При получении алюминия электролизом раствора Аl2О3, в расплавленном криолите пропускают ток 2·104 А. Определить время, в течение которого выделится 10 кг алюминия. k = 1,118·10-6 Кл/моль – электрохимический эквивалент алюминия. |
|
| Какие процессы происходят в гальванических элементах? |
| Укажите типы химических источников тока. |
|
| Емкость батареи аккумуляторов 150 А·ч. За какое время израсходуется весь заряд аккумулятора при среднем разрядном токе 0,3 А? |
| Как называется количество электричества, которое может отдать источник при разрядке до конечного напряжения. |
| Назовите единицу измерения емкости химического источника тока? |
| С какой скоростью ударяется электрон об анод катодной трубки (двухэлектродная трубка), если между ее электродами поддерживается напряжение 220 В? e = 1,6·10-19Кл, me = 9,1·10-31 кг. |
|
| Зарядка аккумулятора продолжалась tз = 5 ч при средней силе тока Iз = 1 А и напряжении Uз = 3 В. Аккумулятор, работая в постоянном режиме, полностью разрядился за tp = 75 ч при силе тока tр = 0,2 А и внешнем сопротивлении R = 4 Ом. Не учитывая внутреннего сопротивления аккумулятора, определить его КПД. |
| Емкость аккумуляторной батареи 80 А·ч при ЭДС ε = 2 В. Сколько энергии потребуется для зарядки этой батареи, если ее КПД η = 60%? |
| Определить емкость аккумулятора, если при средней силе тока 0,8 А полная разрядка произошла через 20 ч. |
| От чего зависит ЕДС элемента Вольта? |
|
| Как изменится ЭДС гальванического элемента Вольта, если его электроды наполовину вынуть из электролита? |