| Сопоставьте внутренние энергии аргона и гелия, находящихся при одинаковых условиях и имеющих одинаковые массы. (Молярные массы μAr = 40 г·моль-1, μНе = 4 г·моль-1). |
| Молярная масса кислорода 0,032 кг/моль. Чему равна масса (кг) молекулы кислорода? NA = 6·1023 моль-1. |
|
| Чему равно отношение среднеквадратичной скорости атомов гелия к среднеквадратичной скорости атомов кислорода при одинаковых условиях? Масса атомов гелия в 4 раза меньше массы атома кислорода. |
| Найдите концентрацию молекул одноатомного газа при его давлении 2Мпа, если средняя кинетическая энергия их поступательного движения 1·10-12 Дж. |
|
Найдите среднюю молярную массу смеси газов, если половину массы газа составляет газ с молярной массой μ1 = 1, а другую половину - газ с массой μ2 = 2.
Выбери ответ
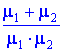 | 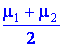 | 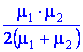 | 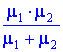 | 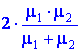 |
| Как изменится энергия одноатомного газа, если давление газа увеличить в 3 раза, а объём уменьшить в 2 раза? (m - const). |
| Чему равна средняя кинетическая энергия поступательного движения молекул одноатомного газа при температуре 300°К? (k = 1,38·10-23Дж/К). |
|
| Вычислить концентрацию молекул газа при нормальных условиях (Т = 273°К, k = 1,38·10-23 , р = 101 кПа)? |
|
| Как изменится давление идеального газа, если увеличить концентрацию молекул в три раза при неизменном значении их средне - квадратичной скорости? |
| Как изменится средняя квадратичная скорость теплового движения молекул идеального газа, если плотность газа увеличить в 9 раз, а давление газа уменьшить в 9 раз? |
| Чему равно изменение внутренне энергии трёх молей идеального газа, если Т1 = Т и Т2 = 3·Т? |
| Сколько молекул содержится в 1 г воды? Число Авогадро принять равным 6·1023 моль-1. |
| Сравнить средние скорости теплового движения молекул кислорода v1, азота v2 и водорода v3 при одинаковой температуре. |
Выбери ответ |
| Сравнить внутренние энергии 1 моля неона (UNe) и 1 моля аргона (UAr) при одинаковой температуре. Атомные массы неона и аргона соответственно равны 20 и 40 атомных единиц массы. Учесть, что оба газа одноатомны. |
|
| Чему равна средняя кинетическая энергия молекул одноатомного газа при давлении р = 8·105 Па, если в 1 м3 этого газа находится 3·1027 молекул? |
|
| Физический смысл постоянной Больцмана [k] состоит в том, что она связывает внутреннюю энергию газа с … |
| Опыт О. Штерна позволил определить |
| Во сколько раз изменяется число молекул в веществе при уменьшении его массы в 91 раз, молярной массы такще в 91 раз ? |
Что изображает график, показанный на рисунке ? |
| Во сколько раз изменяется абсолютная температура идеального газа при увеличении его давления в 10,35 раза и уменьшении его объёма в 3,45 раза ? |
| Давление идеального газа 4,2 МПа, плотность его 1,4 кг/м3. Определите среднюю квадратичную скорость (м/с) молекул газа. |
Какой физической величине численно равна заштрихованная площадь, показанная на рисунке ? |
| Определите массу воздуха m, находящегося в аудитории высотой h = 5 м, если площадь пола равна 200 м2. Температура здания 17 ° С, давление воздуха 105 Па, масса одного киломоля воздуха 29 кг. |
|
| Укажите уравнение Менделеева - Клайперона |
|
| Во сколько раз больше молекул содержится в 36 г воды, чем в 2 г водорода ? |
|
| Сопоставьте давления кислорода и водорода, если концентрация и среднеквадратичные скорости их молекул одинаковы. |
| В трёх сосудах одинакового объёма содержатся по 1 молю Н2, О2 и СО2. Каково соотношение давлений газов, если они имеют одинаковую температуру ? |
| Во сколько раз отличается плотность кислорода ( О2 ) при одинаковых условиях от плотности азота ( N2 ) ? |
| Повышение абсолютной температуры идеального газа в 2 раза привело к увеличению его объёма в 2 раза. Как изменилось его давление ? |
| Определить массу одной молекулы кислорода О2. Молярная масса кислорода М = 32·10-3 кг/моль, NA = 6,02·1023моль-1. |
|
| Выразить массу молекулы воды в килограммах, если известно, что её односительная молярная масса равна 18 а.е.м. |
|
| Сколько молекул воздуха содержится в комнате объёмом 60 м3 при нормальных условиях? Молярная масса воздуха М = 29·10-3кг/моль, плотность воздуха ρ = 1,29 кг/м3. |
| Сколько молекул сернистого газа SO2 содержится в в 1 кг при нормальных условияз? М(S) = 32 г/моль? M(O) = 16 г/иоль, NA = 6,02·1023моль-1. |
| Определите массу молекулы азота N2. M(N) = 14 г/моль. NA = 6,02·1023моль-1. |
|
| В балоне находится 20 моль газа. Сколько молекул газа находится в балоне? NA = 6,02·1023моль-1. |
| При охлаждении газа в замкнутом сосуде: |
| Установите соответствие между физическими величинами и их возможными изменениями в следующей ситуации: при постоянном давлении некоторая масса газа сжимается. Как при этом изменяются температура газа, его концентрация и внутренняя энергия? | Выбери ответ |
| При каких процессaх остаётся неизменной внутренняя энергия 1 моль идеального газа? |
|
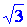 раз.
раз.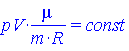 .
.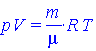 .
.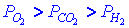 .
.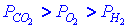 .
.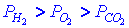 .
.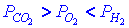 .
.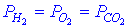 .
.